Jedinečné technologie identifikace zařízení automatizují čtení lékařských ID a čárových kódů
Contributed By DigiKey's North American Editors
2023-10-26
V roce 2013 zavedl americký Úřad pro kontrolu potravin a léků (FDA) systém jedinečné identifikace zdravotnických prostředků neboli UDI. Cílem tohoto pravidla bylo zlepšit bezpečnost pacientů poskytováním konzistentního způsobu sledování a identifikace zdravotnických prostředků pomocí moderní dokumentace v místech výroby, distribuce a použití. Podobně jako požadavky předpisů pro zdravotnické prostředky v Evropě nebo podobné předpisy v jiných zemích, pravidlo UDI v USA zvyšuje přesnost hlášení a usnadňuje analýzu v případě stažení nebo nežádoucí příhody.
Od 24. září 2023 bude úřad FDA na štítcích a obalech zdravotnických prostředků plně vyžasovat národní kódy zdravotnických položek a kódová čísla léků. Jakékoli zdravotnické produkty označené k tomuto datu nebo později musí plně vyhovovat mandátům UDI. Tento mandát se bude týkat následujících produktů:
- Životně kritické produkty třídy 3, jako jsou kardiostimulátory a implantované protetiky
- Středně kritické produkty třídy 2, jako jsou injekční stříkačky, katétry a vstřebatelné stehy
- Produkty třídy 1 s nižším rizikem, jako jsou zubní nitě, lékařské pláště a kyslíkové masky
Plné vyžadování mandátu znamená, že pokud zdravotnický prostředek nemá čitelný čárový kód, nebude nadále považován za platný/použitelný produkt, i když na něm budou umístěny štítky čitelné pro člověka a i když lze produkt obecně považovat za snadno identifikovatelný pro většinu uživatelů. Toto plné vyžadování povede ke komplexnímu přijetí mandátu ve zdravotnictví a ve fakturaci zdravotního pojištění.
 Obrázek 1: některé ruční ověřovače čárových kódů DPM (přímé označování dílů) jsou vybaveny pokročilým osvětlením a dalším softwarem pro automatické vyhledání symbolů a procházení nastavení pro optimalizaci čtení konkrétní značky DPM a substrátu materiálu, který je k dispozici. Zde znázorněný ověřovač LVS-9585 může ve skutečnosti ověřovat díly DPM i tištěné štítky pro účely komplexní analýzy a hlášení. (Zdroj obrázku: Omron Automation)
Obrázek 1: některé ruční ověřovače čárových kódů DPM (přímé označování dílů) jsou vybaveny pokročilým osvětlením a dalším softwarem pro automatické vyhledání symbolů a procházení nastavení pro optimalizaci čtení konkrétní značky DPM a substrátu materiálu, který je k dispozici. Zde znázorněný ověřovač LVS-9585 může ve skutečnosti ověřovat díly DPM i tištěné štítky pro účely komplexní analýzy a hlášení. (Zdroj obrázku: Omron Automation)
Odpovědný je zadavatel (nositel značky).
V USA je za přesnost a kvalitu kódů UDI odpovědný vlastník IP a uživatelská značka každého zdravotnického produktu. To je zvláště důležité, protože velká část trhu s zdravotnickými produkty je vyráběna na základě smlouvy a zajišťována externími zařízeními jiných organizací. Proto je odpovědností smluvní organizace zajistit, aby celý její dodavatelský řetězec vyhovoval UDI a vyráběl přesné štítky.
Unikátní původ technologie identifikace zařízení
UDI jsou statické identifikátory prostředků. Změny množství položek v balíku však mohou vyvolat potřebu nového identifikátoru. Vydávající agentury diktují, jak se tyto podrobnosti rozlišují. Stejným způsobem může změna podmínek sterility balení zařízení také změnit identifikátor zařízení. Změna cílového trhu zařízení (země, kde bude zařízení prodáváno), jazyka štítku nebo označení CE může také vyžadovat změny identifikátoru zařízení.
Před pravidlem UDI mohl výrobce lékařského zařízení označit produkt konkrétním objednacím číslem. Distributor by toto objednací číslo změnil dříve, než by je znovu změnil poskytovatel zdravotní péče nebo nemocnice. Vzhledem k tomu, že každý subjekt mohl změnit objednací číslo dříve, než se dostane k pacientovi, bylo téměř nemožné sledovat produkty, vyřizovat stažení z trhu, zabránit padělání nebo přesně a efektivně objednat nové zásoby.
Související článek: Implementace robustních řešení sledovatelnosti
V současné době je každému zařízení přidělován standardizovaný a trvalý identifikátor, nazývaný UDI, který všem subjektům umožňuje rychlejší a přesnější identifikaci zařízení, což v konečném důsledku snižuje lékařské chyby. Tento identifikátor UDI je tvořen alfanumerickým kódem obsahujícím dva klíčové údaje:
- Identifikátor zařízení
- Identifikátor výroby
Identifikátor zařízení je statický štítek přiřazený danému zařízení uvádějící označovatele (obvykle výrobce zařízení) a konkrétní číslo modelu zařízení. Naproti tomu identifikátor výroby obsahuje data, která se mohou lišit, a velká část dat, která může obsahovat, je volitelná. Ty mohou zahrnovat kódy šarží a dávek, sériová čísla, data expirace a výroby. Stručně řečeno, volitelnými údaji může být cokoliv, co výrobce nebo výrobce štítků považuje za nezbytné pro podporu sledování zařízení.
Každý štítek s identifikátorem UDI musí tyto informace uvádět ve dvou formách:
- Formulář čitelný člověkem (prostý text)
- Strojově čitelný formulář (čitelný čárovým kódem nebo čtečkou RFID)
Všude tam, kde zařízení může uspokojovat více lékařských aplikací, musí být identifikátor UDI umístěn přímo na zařízení, nikoli na jeho obalu. Pravidlo platí i pro zařízení, která lze používat opakovaně.
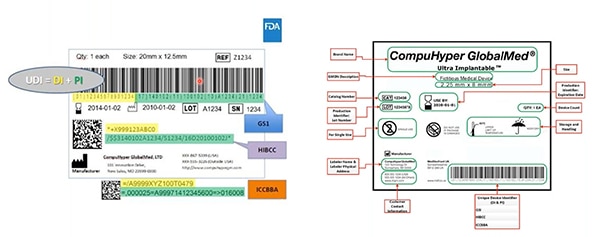 Obrázek 2: orgány vydávající identifikátory UDI podle standardů GS1, HIBCC a ICCBBA vytvářejí identifikátory UDI; přidělují povolenou symboliku UDI; definují, které technologie mohou komunikovat identifikátory UDI komunikovat; a specifikují požadovanou kvalitu značek UDI. Žlutě zvýrazněný na tomto vzorku je identifikátor zařízení; zeleně zvýrazněné jsou identifikátory výroby. Mezi další prvky patří informace čitelné pro člověka… a ty jsou také zakódovány do strojově čitelného čárového kódu. (Zdroj obrázku: FDA)
Obrázek 2: orgány vydávající identifikátory UDI podle standardů GS1, HIBCC a ICCBBA vytvářejí identifikátory UDI; přidělují povolenou symboliku UDI; definují, které technologie mohou komunikovat identifikátory UDI komunikovat; a specifikují požadovanou kvalitu značek UDI. Žlutě zvýrazněný na tomto vzorku je identifikátor zařízení; zeleně zvýrazněné jsou identifikátory výroby. Mezi další prvky patří informace čitelné pro člověka… a ty jsou také zakódovány do strojově čitelného čárového kódu. (Zdroj obrázku: FDA)
Všechna zařízení musí být registrována v globální databázi identifikátorů UDI, aby bylo možné sledování v případě stažení a aby měla k informacím o daném zařízení přístup veřejnost. Vydavatelské agentury akreditované úřadem FDA jsou oprávněny vytvářet jedinečné identifikátory, které výrobci zařízení umístí na své produkty.
Související bílá kniha: Aktuální informace o sledovatelnosti
Technologie a techniky skenování identifikátorů UDI
Štítky UDI lze během jejich cesty od výroby k použití ověřovat několika způsoby.
Inline ověřování je prováděno technologiemi integrovanými do větších strojních zařízení, aby bylo zajištěno rychlé a přesné zpracování velkého množství produktů při jejich výrobě. S podporou pokročilého softwaru mají tyto technologie příležitostně podobu průmyslových tiskáren štítků. Tyto tiskárny jsou schopny provádět vlastní inline ověřování, aby se potvrdilo, že informace v identifikátoru UDI jsou čitelné podle náročných průmyslových standardů ihned po jejich vytvoření v místě výroby štítků. Například verifikátory Omron Automation V275 jsou určeny pro použití s termálními tiskárnami Zebra, aby vyhovovaly normě ISO 15426 a standardům GS1 vydávajícího orgánu pro zajištění shody s požadavky úřadu FDA.
Související článek: Řešení sledovatelnosti Omron
V jiných případech má inline ověřování podobu specializovaných lemovacích dopravníků se strojovým viděním na automatizovaných výrobních linkách, které zahrnují čtení čárových kódů pro extrémně rychlé a přesné ověřování UDI značení na high-mix produktech na vysokorychlostních výrobních linkách. V této oblasti vynikají nabídky čteček skupiny MicroHAWK od společnosti Omron Automation díky pokročilým senzorům doplněným miniaturizovanou konstrukcí a možnostmi konektivity zahrnujícími Ethernet/IP a PROFINET.
Související článek: Vyhněte se odpovědnosti za nesprávné značení
Naproti tomu offline ověřování identifikátorů UDI je nejvhodnější pro dávkové vzorkování štítků pro zajištění kvality. Offline ověřování, které se často používá pro testování vzorků v době, kdy zdravotnické prostředky opouštějí zařízení nebo do něj vstupují, může doplňovat online ověřovací systémy před distribuční cestou.
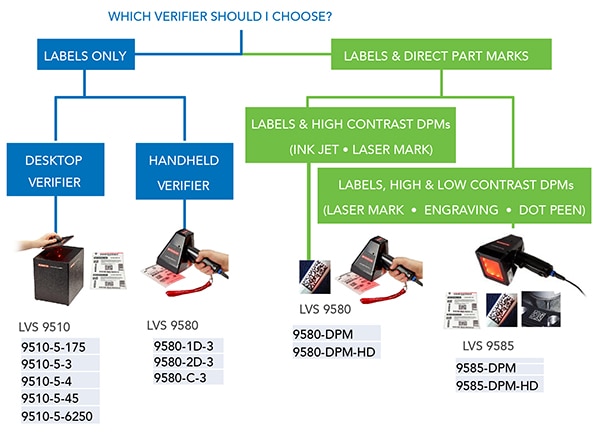 Obrázek 3: identifikátory UDI umístěné přímo na produktech vyžadují jiné čtečky než identifikátory UDI vytištěné na nalepených štítcích. (Zdroj obrázku: Omron Automation)
Obrázek 3: identifikátory UDI umístěné přímo na produktech vyžadují jiné čtečky než identifikátory UDI vytištěné na nalepených štítcích. (Zdroj obrázku: Omron Automation)
Používání ověřovačů kompatibilních s normou ISO může být ve skutečnosti výhodné pro všechny provozy zdravotnické distribuce a péče. Uvažme offline produkty Omron pro ověřování identifikátorů UDI řady LVS 95XX. Tyto produkty se používají:
- Na laserových označovacích stanicích a tiskárnách štítků, kde se vytvářejí kódy.
- V místech aplikace kódů na produkty, které mohou, ale nemusí být oddělené od oblastí tvorby kódu.
- Ve stanicích kontroly kvality, kde se potvrzují šablony, formátování a další kódovací prvky.
Specifikace variant offline ověřovače identifikátorů UDI
Nejvhodnější offline ověřovač identifikátorů UDI pro danou aplikaci závisí na několika parametrech.
Velikost čárového kódu: velké čárové kódy se často snáze snímají, protože identifikátory mají velké zorné pole definované ohniskovou vzdáleností čočky a velikostí snímače. Uvažme stolní identifikátory UDI LVS-9510 od společnosti Omron Automation. Tato řada produktů dokáže číst jak lineární, tak i 2D štítky. Jelikož existuje pět různých verzí s odlišnámi zornými poli, mohou konstruktéři mohou zvolit tu, která bude kompatibilní s velikostí čárového kódu určeného k ověření. Funkce spojování umožňuje klasifikaci čárových kódů přesahujících zorné pole.
Kromě toho mohou všechny ověřovače LVS-9510 automaticky stanovit symboliku a aperturu potřebnou k vyhodnocování kódů a identifikaci/zvýraznění problematických míst.
 Obrázek 4: čtení čárových kódů vyhovujících normám ISO je jednodušší díky zařízení schopnému číst lineární (1D) i dvourozměrné (2D) kódy. Některá taková zařízení určují symboliku a aperturu potřebnou k vyhodnocení kódů a identifikují a zvýrazňují problémy. Zde zobrazený ověřovač LVS-9510 používá funkci spojování, která umožňuje klasifikaci čárových kódů větších, než je zorné pole. (Zdroj obrázku: Omron Automation)
Obrázek 4: čtení čárových kódů vyhovujících normám ISO je jednodušší díky zařízení schopnému číst lineární (1D) i dvourozměrné (2D) kódy. Některá taková zařízení určují symboliku a aperturu potřebnou k vyhodnocení kódů a identifikují a zvýrazňují problémy. Zde zobrazený ověřovač LVS-9510 používá funkci spojování, která umožňuje klasifikaci čárových kódů větších, než je zorné pole. (Zdroj obrázku: Omron Automation)
Typ čárového kódu: skenery musejí umět číst čárové kódy přidělené vydávajícími orgány ve formátech známých jako HIBCC, ICCBBA nebo (nejčastěji od roku 2023) GS1. Standard GS1 určuje velikost, formát a rozlišení kódů UPC, lineárních čárových kódů a 2D datových maticových čárových kódů.
Umístění značky UDI: uvažme přímé označování dílů (DPM) zdravotnických prostředků. Tyto značky mohou být mimořádně malé, zvláště tehdy, poku identifikují chirurgické nástroje a implantovatelné zdravotnické prostředky. Pro zajištění čtení a ověřování takových kódů DPM UDI jsou ruční ověřovače Omron LVS-9580 a LVS-9585 s ultravysokou hustotou vybaveny specializovanou čočkou, která dokáže vyhodnocovat nesčetné množství kódů DPM, včetně těch s velikostí buněk až 0,002 palce. Průmyslové čočky uvnitř čteček LVS-9580 a LVS-9585 zajišťují konzistentní přesnost čtení. Nejsofistikovanější jsou vysoce ovladatelné a kalibrovatelné světelné technologie uvnitř skenerů. Osvětlení umožňuje společně s více zornými poli okamžitou optimalizaci pořízených snímků UDI. To je zvláště důležité, protože standard kódu neumožňuje žádné následné opravy nebo manipulace s obrázky.
Více o softwaru skeneru UDI
Prodosažení maximální efektivity musí UDI software na podporu hardwaru ověřovače prezentovat diagnostické informace v intuitivním formátu. Tento software musí vyhodnocovat kódy UDI podle parametrů definovaných normou ISO (což je nejdůležitější pro potvrzení jeho čitelnosti) a v ideálním případě by měl také sledovat zhoršující se problémy během série skenů UDI.
Společnost Omron zahrnuje veškerý potřebný software s každým hardwarem pro skenování identifikátorů UDI. Software je pravidelně aktualizován, aby držel krok s rychle se vyvíjejícími předpisy a novou průmyslovou legislativou.
Hlavní funkcí softwaru skeneru Omron je zpracování syntaxe kódu. Stručně řečeno, každý čárový kód nebo 2D kód musí přesně extrahovat všechny příslušné informace včetně typu produktu, čísla šarže, množství podle potřeby, data expirace, informací o dodání atd. Výsledné datové řetězce musí být naformátovány konkrétním způsobem, aby udržely krok s vyvíjejícími se požadavky, metodikami a destinacemi lékařských produktů.
Pravidelně aktualizovaný software výrobcem skeneru poskytuje koncovým uživatelům aktuální informace i při vydání nových kódů.
Závěr
Americká armáda kdysi chtěla plně využívat systém sledování produktů UID, který je podobný systému UDI ve zdravotnictví. Jeho účelem bylo omezit obrovské plýtvání spojené se ztrátami, duplikacemi a nepočítanými dodávkami ve vojenských zařízeních, včetně všeho od hotových zbraní Raytheon až po řídicí desky dodávané malou firmou pro určité specializované aplikace. Dnes mají systémy UID různé úrovně použití.
Osud mandátu UDI však nebude stejný.
Mantra, která řídí přijetí UDI, je přímočará: Štítek je produkt. Nesprávné označení totiž může vyvolat řetězec událostí, které plýtvají časem zdravotnického personálu a mají za následek ztrátu zdravotnického prostředku. Identifikátory UDI proto musejí být umístěny na všech vrstvách obalu, například na úrovni jednotky, balíku, svazku, krabice a palety. Identifikátory UDI na sterilních zdravotnických prostředcích uvnitř sterilizačních pečetí jsou obzvláště důležité, protože porušení pečeti za účelem ověření typu zařízení je nepřípustné.
Vzhledem k tomu, že úřad FDA od 24. září 2023 vyžaduje plné dodržování směrnic UDI, stanou se pokročilé skenovací technologie pro ověřování zdravotnických produktů prvořadé pro výrobce automatizace i pro výrobce strojů a koncové uživatele, kterým slouží.
Takové skenery mohou splňovat extrémně specifické požadavky úřadu FDA na identifikátory UDI pro potvrzování štítků na široké škále laboratorních, lékařských a klinických diagnostických zařízení. Offline ověřovače čárových kódů maximalizují sledovatelnost, inline strojové vidění a obsahují pokročilé čtečky kódů DPM.

Disclaimer: The opinions, beliefs, and viewpoints expressed by the various authors and/or forum participants on this website do not necessarily reflect the opinions, beliefs, and viewpoints of DigiKey or official policies of DigiKey.






